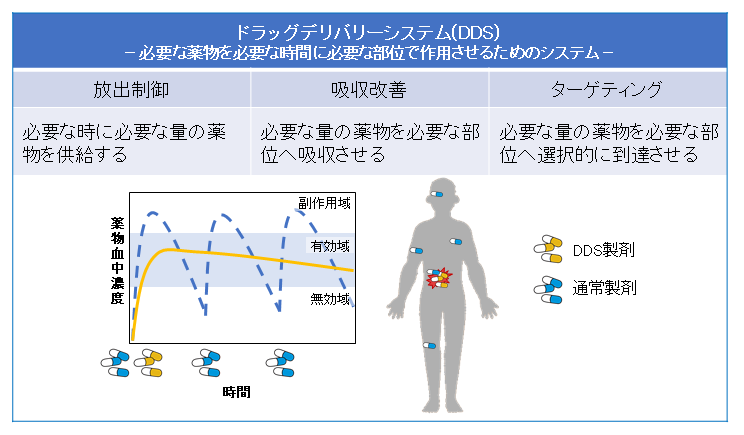
3つの要素技術からなる『ドラッグデリバリーシステム』
(2020年2月01日)
創薬の現場では、モダリティ(治療手段)の多様化が進んでいます。治療標的に効果的に作用するモダリティが探索され、医薬品の代表格であった低分子化合物に加えて抗体を含むタンパク質、中分子化合物、ペプチド、核酸、細胞など様々なものが検討されています。しかし、どんなモダリティも標的部位に正しく送達されなければならない点は、共通の課題です。この課題に対して、必要な薬物を必要な時間に必要な部位で作用させるためのシステムであるドラッグデリバリーシステム(Drug Delivery System, DDS)が開発されています。ここでは、既に臨床的に活用されている事例を含め、DDSの3つの要素技術についてご紹介します。
放出制御
医薬品には1日3回水で服用や1回1~2滴、1日3~5回点眼といった用法・用量が定められています。薬は多く使い過ぎると副作用の危険があり、少な過ぎると効きません。安全に効果が得られる適正な使い方として決められていますので、用法・用量は遵守することが求められます。しかし、忙しい毎日の中で薬を飲み忘れてしまったり、飲む時間がなかったりすることは少なくありません。そこで、薬物を体内へ供給する速度を制御することで、1回の投薬で長時間に渡って有効性を維持する放出制御技術が開発されています。1日1回の服用で済む薬の多くに放出制御技術が使われています。より長期間に渡る放出制御を実現している医薬品として、注射用リュープロレリン酢酸塩という前立腺がんなどに使われる薬があります。この薬は微粒子に含有された状態で皮下に投与されます。皮下に留まった微粒子は徐々に分解するようになっており、この分解に従って薬物が放出される仕組みです。微粒子の成分によって分解速度を調整することができ、最長で6ヶ月に1回の投与でも薬効が維持できる製剤が販売されています。
長く服用することが分かっているすべての薬に放出制御技術を活用することで利便性が増す訳ではありません。例えば1ヶ月に1回投与を実現しようとすると1ヶ月分の薬をまとめて投与することになりますから、用量が多い薬の長期放出では逆に投薬が難しくなってしまう場合があります。また、アクシデントで薬物全量が一気に放出されてしまうといったことがないよう、確実な製剤設計が必要です。
吸収改善
同じ効果を示す薬で口から飲むものと注射するものがあったら、飲み薬を選択する人が多いと思います。しかし、タンパク質や核酸など薬の分子量が大きいものや消化酵素で分解され易いものなどは消化管から吸収されにくいため、注射で投与するしかありません。そこで、このような薬物吸収のバリアを突破するための吸収改善技術が開発されています。闇雲にバリアを破壊すると薬以外の病原体なども吸収されてしまいますので、安全性に配慮した精密な技術設計が必要です。これまでに様々な吸収促進法が検討されてきましたが、2019年にサルカプロザートナトリウム(SNAC)という吸収促進剤を添加したセマグルチドの経口薬が米国で承認されたことに注目が集まっています。セマグルチドは優れた糖尿病治療薬ですが消化管で分解されやすいペプチドであるため、これまで注射剤しかありませんでした。SNACとセマグルチドが相互作用して分解から守るとともに、胃の粘膜を透過しやすい構造となって吸収されると考えられています。
SNACなどの吸収促進剤は万能にあらゆるモダリティの経口投与を可能にする訳ではありません。また、食事の影響を受けて吸収性が低下するなどの課題も指摘されています。患者にとって身体的にも精神的にも負担が大きい注射薬を全て経口投与可能にする技術の登場には、もう少し時間が掛かりそうです。
ターゲティング
体内に吸収された医薬品は血流に乗って全身に分布します。治療の目的以外の場所にも薬は分布しますので、副作用の原因となります。そこで、薬物を目的の場所だけに届けるターゲティング(標的指向化)技術が求められています。特定の標的(抗原)と特異的に結合する性質を持つ抗体を薬物の運び手として利用して、がん特異的抗体に抗がん剤を化学結合させた抗体-薬物複合体の研究・開発が盛んに行われています。高い殺細胞効果をもつ薬の行き先を抗体の標的(例えば、がん細胞)選択性で限定しますので、副作用のリスクが低く、強い薬効を示すことが期待されています。抗体-薬物複合体は既に国内で4品目、米国では7品目が承認されており、100品目近くが臨床開発段階にあります。
抗体以外にも肝臓の細胞に特異的に発現している受容体と強く結合する分子を使ったターゲティングなども臨床的に使われています。製造の手間やコストも考慮して、標的に応じたターゲティング用の運び手はさらに進化していくと期待されます。
DDSは対象とする疾患、医薬品モダリティ、放出制御・吸収改善・ターゲティングの目的によって様々なニーズに応えることが求められています。今後、さらに精緻なDDSの具現化には、研究分野の垣根を超えた学際的連携をいっそう深めた集学的アプローチが必要不可欠だと考えています。
参考資料
- JST CRDS 研究開発の俯瞰報告書 ライフサイエンス・臨床医学分野(2019年)
2.1 基礎基盤科学技術 -分子・細胞、 2.5 健康・医療 - JST CRDS 研究開発の俯瞰報告書 ナノテクノロジー・材料分野(2019年)
2.2 ライフ・ヘルスケア応用 - JST CRDS 俯瞰ワークショップ報告書 次世代医薬・基盤技術の動向と展望、推進すべき研究開発戦略(2019年)

中村 輝郎(なかむら てるお)
東京理科大学大学院材料工学専攻修士課程を修了後、中外製薬株式会社入社。DDS技術開発などに従事。2019年より国立研究開発法人科学技術振興機構研究開発戦略センターに出向。ライフサイエンス・臨床医学・製薬関連分野における技術動向や社会動向の俯瞰調査および政策提言の作成に従事。